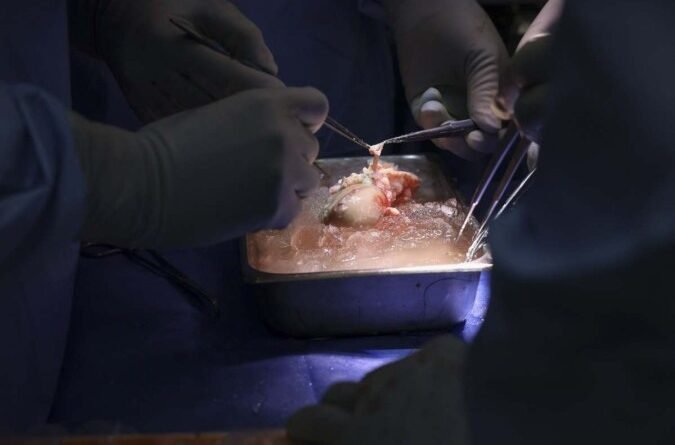
Entenda como ocorreu o primeiro transplante de rim de porco para humano
CB – Médico brasileiro comanda equipe que realizou com sucesso a cirurgia inédita e revolucionária, que transferiu o órgão geneticamente modificado para um homem vivo, de 62 anos, com doença crônica renal, em Massachusetts, nos EUA.
Na tarde de ontem 42.462 pessoas esperavam por um transplante de órgão no Brasil, do total, 39.187 aguardavam um rim. Horas antes, profissionais da saúde do Massachusetts General Hospital (MGH), nos Estados Unidos, liderados pelo médico brasileiro Leonardo Riella, anunciaram o primeiro transplante bem-sucedido do mundo de um rim de porco geneticamente modificado em um paciente vivo. O órgão foi transferido a um homem de 62 anos que tem uma doença renal em estágio avançado. Para especialistas, o feito é um passo gigante em direção a um novo modo de salvar vidas. A cirurgia durou cerca de quatro horas e foi realizada em 16 de março.
O procedimento foi coordenado por Leonardo Riella, brasileiro, diretor médico de Transplante Renal, Tatsuo Kawai, diretor do Centro Legorreta para Tolerância Clínica a Transplantes e Nahel Elias, chefe Interino de Cirurgia de Transplante e diretor de Cirurgia de Transplante de Rim. O rim de porco usado no transplante passou por 69 edições genéticas antes da operação.
“Setenta anos após o primeiro transplante renal e seis décadas após o advento dos medicamentos imunossupressores, estamos à beira de um avanço monumental no transplante. Só no MGH, há mais de 1.400 pacientes em lista de espera para transplante renal. Infelizmente, alguns morrerão ou ficarão doentes demais para serem transplantados devido ao longo tempo de espera na diálise. Estou firmemente convencido de que o xenotransplante representa uma solução promissora para a crise de escassez de órgãos”, ressaltou Riella.
O rim animal foi fornecido pela Genesis de Cambridge, nos Estados Unidos, a partir de um porco geneticamente editado usando a tecnologia CRISPR-Cas9 para remover genes suínos prejudiciais e adicionar certas partes de DNA humano para melhorar a compatibilidade com pessoas. Além disso, os cientistas inativaram retrovírus suínos presentes no animal, para eliminar qualquer risco de infecção no paciente. Nos últimos cinco anos, o MGH e a eGenesis conduziram extensas pesquisas colaborativas, com as descobertas publicadas na Nature em 2023.
Raphael Rebello, nefrologista da clínica Renal Mais, em Brasília, destaca que a inativação dos retrovírus endógenos do porco é muito importante porque uma das principais preocupações é a transmissão de infecções do suíno para o ser humano. “Não só retrovírus, mas existem verminoses e outros possíveis patógenos. Os retrovírus, muitas vezes, se proliferam em situações onde há imunossupressão e o espalhamento é muito rápido, por isso é importante a inativação, mas ainda não sabemos, a longo prazo, em um ser humano vivo, as consequências disso.”
Entre outras modificações necessárias no órgão, Giulia Hatae, nefrologista da Beneficência Portuguesa (BP), de São Paulo, enfatiza a retirada de três genes responsáveis pela rejeição rápida, mediada por anticorpos. “Entre as principais dificuldades nessa área, estão as questões éticas de segurança, bem como a necessidade de pesquisas mais aprofundadas para garantir a eficácia e segurança do procedimento. O Brasil tem um sistema extremamente burocrático, o que acarreta uma morosidade em sobrepujar essas etapas, dificultando a acessibilidade da população a algo que pode ser revolucionário do ponto de vista econômico e na qualidade de vida dos pacientes”, disse.
O procedimento bem sucedido em uma pessoa viva é um marco na área do xenotransplante — transplante de órgãos ou tecidos de uma espécie para outra —, que surge como uma solução potencial para a falta de órgãos doados em todo o mundo.
Forte e corajoso
Conforme divulgado pelo hospital, o paciente, Richard Slayman, está se recuperando bem e, em breve, terá alta. Com um histórico de saúde complexo, ele tem diabetes tipo 2 e hipertensão, já havia recebido transplante de doador humano. O rim mostrou sinais de falha aproximadamente cinco anos depois e ele retomou a diálise em maio de 2023. Quando voltou a realizar o procedimento, teve complicações, sendo necessário ir ao hospital a cada duas semanas para descoagulação e revisões cirúrgicas, o que impactou significativamente sua qualidade de vida.
Slayman se manifestou em um comunicado, reafirmando sua convicção nos profissionais. “O nefrologista Winfred Williams e a equipe do Transplant Center sugeriram usar o porco, explicando os prós e os contras. “Eu vi isso não apenas como uma forma de me ajudar, mas também de dar esperança às milhares de pessoas que precisam de um transplante para sobreviver. Quero agradecer a todos no MGH que cuidaram de mim”, disse ele no texto.
“O verdadeiro herói hoje é o senhor Slayman, pois o sucesso dessa cirurgia pioneira, antes considerada inimaginável, não seria possível sem a sua coragem e vontade de embarcar numa viagem a um território médico desconhecido. (…) Ele se torna um farol de esperança para inúmeros indivíduos que sofrem de doença renal em fase terminal”, afirmou Joren Madsen, diretor do Centro de Transplantes do MGH.
Williams destacou a relevância do transplante. “O sucesso contínuo desse transplante renal inovador representa um verdadeiro marco e um avanço potencial na resolução de um dos problemas mais intratáveis no nosso campo, o acesso desigual dos pacientes de minorias étnicas à oportunidade de transplantes renais devido à extrema escassez de órgãos de doadores e outras barreiras baseadas no sistema.”
O procedimento foi realizado sob um único Protocolo de Acesso Expandido — conhecido como uso compassivo — concedido a um único paciente ou grupo de pacientes com doenças ou condições graves e potencialmente fatais para obter acesso a tratamentos experimentais ou ensaios, quando não houver tratamento comparável. Slayman também recebeu infusão de novos medicamentos imunossupressores.
Murilo Morelli, nefrologista da clínica NefroStar, em Brasília, pontua que um desafio é a rejeição do órgão transplantado pelo sistema imunológico do receptor. “Isso já é uma questão mesmo nos transplantes entre pessoas e se torna mais complicado no caso do xenotransplante. Existe a necessidade de grandes investimentos na área de terapias celulares como a construção de biotérios para produção desses animais.”